همفری دیوی

تولد دیوی
"همفری دیوی" ، دانشمند انگلیسی در 17 دسامبر سال 1778 در پنزانس در انگلیس بدنیا آمد. دیوی پسر ارشد خانواده اش بود که از طبقه متوسط جامعه بودند.
تحصیل علم و دانش
او تحصیلات ابتدایی را در مدرسه گرامر که در نزدیکی پنزانس بود آغاز کرد و آغاز تحصیلاتش در سال 1793 بود. دیوی هنگامی که نزدیک داروفروش جراح ، شاگردی میکرد، برنامه خودآموزی شامل الهیات ، جغرافیا ، هفت زبان و تعدادی موضوعهای علمی برای خود طرحریزی کرد، به مطالعه فلسفه پرداخت و از طریق آثار نیکلسن و لاوازیه ، شیمی آموخت.
روحیات و علایق دیوی
او بسیار مهربان و سر زنده بود و قوه تخیل قوی داشت. او دوستدار ترکیب کردن برای ساختن شعر بود. همچنین آتشبازی ، ماهیگیری ، دویدن و جمع آوری مواد معدنی از دیگر تفریحات او بود. یکی از عادات او و علایقش این بود که یک جیبش را با قلاب ماهیگیری پر کند و جیب دیگرش را با نمونههای سنگ که جمع آوری کرده بود. او هرگز علاقه قلبیش به طبیعت را از دست نداد. در جوانی بسیار بیریا و ساده دل بود.
آغاز تحقیقات در دنیای شیمی
– 1827) به او پیشنهاد داد که از کتابخانه اش استفاده کند و به او یک لابراتوار شیمی داد که در آن دوران بسیار نادر و عالی بود. او در آنجا با طبیعت گرما ، نور و الکتریسیته آشنا شد. او در لابراتوار کوچکش گاز نیترو اکسید(گاز خنده آور) را آماده و اسنشاق کرد و ادعا کرد که این گاز ، خواص بیهوش کننده دارد.
دیوی در سال 1807 به عنوان منشی جامعه سلطنتی برگزیده شد. وی در سال 1815 لامپ بیخطری را اختراع کرد که نامش را در تاریخ زنده کرد. این دانشمند انگلیسی در فیزیک و شیمی تحقیقات جالب و جامعی کرد. سدیم، پتاسیم ، کلسیم ، باریم ، منیزیم و استرانسیم را جدا کرد. مطالعاتی در باب گاز خنده آور کرد. در الکتروشیمی بررسیهای عالمانه ای انجام داد. چراغ بیخطری را که دیوی اختراع کرد، خطر انفجار در معادن زغال سنگ را از بین برد.
جداسازی فلزات قلیایی و قلیایی خاکی
اگر چه شیمیدانان از زمان درازی احتمال داده بودند که خاکهای قلیایی ، اکسید فلزهایی باشند، با این حال طبیعت سود و پتاس تا اوائل قرن 19 مورد بررسی قرار نگرفته بود حتی لاوازیه در این مورد ، نظر مشخصی نداشت. او نمیدانست که جزء اصلی سود و پتاس چیست و حدس میزد که ازت یکی از اجزای تشکیلدهنده این مواد است.
به نظر میرسد که این اشتباه از شباهت میان نمکهای سدیم و پتاسیم با نمکهای آمونیوم مایه گرفته است. امتیاز تعیین این اجزا از آنِ دیوی است.
جداسازی پتاسیم و سدیم
ابتدا ناکامی عرصه را بر دیوی تنگ کرده بود، به این معنی که نمیتوانست به کمک یک پیل گالوانیک از سود و پتاس ، فلز استخراج کند.
بزودی وی به خطای خودش پی برد و فهمید که با بکار بردن محلول آبی اشباع شده ، وجود آب مانع از تجزیه نمکها میشود. در اکتبر سال 1807 ، دیوی تصمیم گرفت که پتاس بیآب را ذوب کند و به محض اینکه با این مذاب ، الکترولیز را شروع کرد دانههای کوچک مشابه جیوه و دارای جلای فلزی در روی قطب منفی که در ماده مذاب قرار داشت، ظاهر شدند. برخی از دانهها فوراٌ به حالت انفجاری سوختند و شعله درخشانی پدید آوردند، در حالیکه بقیه آنها آتش نگرفتند، بلکه کدر شدند و با قشر نازک سفیدی پوشیده شدند.
دیوی از تجربههای متعددی که در این زمینه کرد، نتیجه گرفت که آن دانهها همان ماده ای هستند که وی در جستجویش است و این ماده هیدروکسید پتاسیم است که شدیداٌ قابل اشتغال میباشد. دیوی آن فلز را به دقت مورد بررسی قرار داد و متوجه شد که وقتی با آب ، ترکیب میشود، شعله حاصل از واکنش ، ناشی از سوختن هیدروژن آزاد شده از آب است.
وقتی دیوی بر روی فلز تهیه شده از هیدروکسید پتاسیم بررسیهای لازم را انجام داد، به فکر جستجو در هیدروکسید پتاسیم افتاد و با بکار بستن همان روش قبلی موفق به جدا کردن فلز قلیایی دیگری شد. در زمان کوتاهی این دانشمند ، بررسی دقیق خواص پتاسیم و سدیم را به انجام رساند، برخی شیمیدانان درباره طبیعت عنصری سدیم و پتاسیم تردید داشتند و تصور میکردند آن دو ترکیبات قلیاییها با هیدروژن هستند. سرانجام "گی لوساک" و "تنار" بطور واقعی ثابت کردند که آنچه را که دیوی بدست آورده است، در حقیقت عناصر ساده میباشند.
جداسازی فلزات قلیایی خاکی
دیوی ، نخستین بار در سال 1808 ، منیزیم فلزی را بدست آورد. وی برای این کار به همان روشی متوسل شد که برای تهیه سدیم و پتاسیم پیش گرفته بود. گذشته از این عناصر ، دیوی موفق به کشف کلسیم ، باریم و استرانسیم نیز شد. وی ثابت کرد که عناصر شیمیایی به عنوان مواد اصلی قدرت اسیدی یا قدرت قلیایی عمل نمیکنند و نتیجه گرفت که خواص شیمیایی ، تابعی از آرایشهای نسبی و نیز تابعی از ترکیبات مادهاند.
نظریههای دیوی در مورد سایر عناصر
دیوی نشان داد که اکسیژن در واکنشهایش با اسید اوکسی موریاتیک ، هرگز بدون وجود آب تولید نمیشود. وی این اسید را جزو عناصر قرار داد و آن را کلر نامید.
دیوی ، ماهیت و خواص اساسی ید را روشن ساخت.وی فقط با کار سه ماهه در مورد گاز انفجاری آتشدمه ، تائید کرد که ماده اصلی تشکیل دهنده آن ، متان است و فقط در دماهای بالا آتش میگیرد.
مشاغل مهم دیوی
وی همچنین رئیس مؤسسه گازدرمانی "تامس بدوز" در کلیفتن شد. وی پس از 5 سال که اولین کتاب شیمی خود را قرائت کرد، در مؤسسه پادشاهی به تدریس و سخنرانی در شیمی مشغول شد و آنجا را به مرکزی برای تحقیقات پیشرفته تبدیل کرد و خود نیز بیشتر حیات شغلیش را در آنجا گذرانید. دیوی در رساله ای قدیمی به نظریه گرمایی لاوازیه به علت وارد کردن مواد تخیلی و واژه ذهنی گرمایی حمله کرد و نظریه ای داد که در آن ، گرما همچون حرکت و نور به عنوان ماده انگاشته میشد. وی به جای واژه گرمایی عبارت حرکت رانشی را پیشنهاد داد.
مرگ دیوی
دیوی سرانجام در 29 مه سال 1829 در شهر ژنو در سوئیس درگذشت، در حالیکه 51 سال داشت






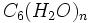 و بسیاری از اجزا سازنده ساده ، کربوهیدراتهای پیچیده دارای فرمول عمومی
و بسیاری از اجزا سازنده ساده ، کربوهیدراتهای پیچیده دارای فرمول عمومی 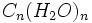 هستند.
هستند. 

 زندگی عبارتست از علم و هنر.
زندگی عبارتست از علم و هنر.